
The work of Prof. Dr. L.W.J. Holleman
Exploring the Science of
Alchemy in Life Processes.
Ein Versuch zur Prüfung des Vorkommens biogener Transmutation
(An Attempt to Examine the Phenomenon of Biological Transmutation)
L.W.J. Holleman
Universität Utrecht 1981
Seit mehr als zwei Jahrhunderten betrachtet man in der Chemie das Prinzip der Erhaltung des Stoffes, insbesondere in der Form der Unveränderlichkeit jeglichen Elementes als absolut gültiges Gesetz. Die Transmutation von Elementen bei chemischen Vorgänge, auch in lebenden Wesen, wird somit als nicht bestehend angesehen. Mit der Entwicklung der Kernchemie im 20. Jahrhundert wurde zwar die Transmutation im anorganischen Bereich ein bekannter und vielfach untersuchter Prozess, ausserhalb dieses Gebietes jedoch gilt sie nach wie vor als unmöglich.
In der Biologie ist allerdings das Erhaltungsgesetz etwas später als in der Chemie zur allgemeinen Anerkennung gekommen; hier waren Anfang des 19. Jahrhunderts die Umsetzung von Elementen in andere als Begleiterscheinung des Lebensprozesses, also die biogene Transmutation und sogar die Neuschaffung von Materie noch geläufige Begriffe.
Mit der Publikation der preisgekrönten Versuche von Wiegmann und Polstorff1 in 1842 wurde auch auf diesem Gebiet das chemische Erhaltungsgesetz massgebend. Seitdem sind während mehr als einem Jahrhundert nur vereinzelte experimentelle Arbeiten über das Thema erschienen, die in dieser Periode völlig unbeachtet blieben.2 Erst in neuerer zeit ist von verschiedener Seite die Möglichkeit einer biogenen Transmutation wieder ins Auge gefasst worden, wenn auch hauptsächlich von theoretischem Standpunkt aus gesehen.3, 4, 5, 6
Eine kritische Betrachtung älterer und neuerer experimentellen Untersuchengen führt aber zu dem Schluss, dass auf diesem Weg bisher ein entscheidendes Resultat weder für noch gegen das Vorkommen der biogenen Transmutation erlangt worden ist.7
Ausserdem gehen die neueren Arbeiten alle vorbei an einer Äusserung von Rudolf Steiner, der bereits 1924 auf Grund geisteswissenschaftlicher Untersuchungen die Umsetzung von Kalium und Calcium über Zwischenstufen in Stickstoff als wesentlichen Moment im organischen Prozess bezeichnete.8 Eine experimentelle Bearbeitung dieser speziellen Angabe ist bisher nicht erschienen. Der unten beschriebene Versuch möchte als ein Beitrag dazu betrachtet werden.
Prinzip der Versuchsanordnung
Die experimentelle Entscheidung zwischen der Gültigkeit des Erhaltungsgesetzes mit Bezug auf bestimmte Elemente einerseits und der Möglichkeit ihrer Verwandlung (Transmutation) unter dem Einfluss eines Lebensprozesses andererseits wird immer hinführen zu einem bestimmten Typus von Versuchen. Man wird dabei eine bekannte Menge, zwecks Homogenität möglichst kleiner Organismen oder Keime, zusammen mit einer ebenfalls genau bekannten Menge einer adäquaten Nährlösung – in einem Gefäss, das die Flüssigkeit bezüglich der zu untersuchenden Bestandteile vollkommen von der Aussenwelt isoliert – der Entwicklung überlassen und nach Verlauf einer angemessenen Zeit die ganze Masse durch quantitative Analyse auf die Unveränderlichkeit des Gehaltes an den betreffenden Elementen prüfen.
Es darf als selbstverständlich betrachtet werden, dass für die zu prüfenden Elemente die für das pflanzliche Wachstum als essentiell geltenden gewählt werden sollen, weil nur diese in tieferem Sinn mit dem Stoffwechselprozess des Organismus verbunden sein dürften.
Um eine eventuelle Abweichung vom Erhaltungsgesetz genauer erfassen zu können, wurde versucht, einen pflanzlichen Mikro-Organismus (Chlorella) in einer einzigen Menge Nährlösung wiederholt zur vollen Entwicklung kommen zu lassen. Dazu wurde je nach einer Wachstumsperiode des Organismus, die 9 bis 14 Tage dauerte, die ganze Masse in Asche übergeführt, diese in Lösung gebracht und nach Herstellung des ursprünglichen Volumens und säuregrades von Neuem mit dem Versuchsorganismus geimpft. Es erwies sich als möglich, diese Wiederherstellung der Wachstumsbedingungen ohne Zusatz von Fremd-Ionen und unter nur geringer Konzentrationserhöhung der Nährlösung durchzuführen. Ausserdem spielte sich der ganze Prozess jeweils ohne Wechsel des Gefässes ab. Ein etwaiger Transmutationseffekt liesse sich bei dieser kumulativen Arbeitsweise im Prinzip beliebig verstärken.
Um den Prozess in der Zeit verfolgen zu können, wurden sechs Teilversuche eingesetzt, deren erster nach einer einzigen Wachstumsperiode abgeschlossen wurde, ein zweiter nach zwei Perioden usw. bis zum sechsten nach sechs Wachstumsperioden.
Für jede Versuchskultur wurde gleichzeitig eine Kontrolle der gleichen Zusammensetzung und unter denselben Bedingungen eingesetzt. Die Behandlung der Kontrollen unterschied sich nur dadurch von derjenigen der Kulturen, dass sie immer gleich nach der Impfung eingedampft und verascht wurden. Bis zum Einsatz der nächsten Wachstumsperiode blieben sie im Exiccator, kamen dann zusammen mit der zugehörigen Versuchskultur zur Bearbeitung usw.
Der Versuch wurde in erster Linie beschränkt auf die Prüfung des Erhaltungsgesetzes für Kalium und Natrium, er soll aber in der Folge auf alle Aschenbestandteile ausgedehnt werden.
Die Einbeziehung des Natriums in den Analysen geschah in der Erwartung, dass es als entbehrliches Element keine wesentliche Bedeutung für den organischen Bildungsprozess hat und daher als rein äusserlicher Bestandteil der Nährlösung dem Erhaltungsgesetz streng folgen wird. Unter dieser Annahme ist es als interner Standard zu verwenden: Volumenänderungen der Kulturflüssigkeit als Ganzes, etwa durch Verdampfung des Lösungswassers oder durch überspritzen aus den Schalen9 usw. würden bei der Analyse erwartungsgemäss keinen Einfluss auf das Verhältnis der Konzentration irgendeines Elementes zu dem des Natriums haben. Eine Änderung dieses Konzentrationsverhältnisses ist daher eine zuverlässigere Andeutung einer Ab- oder Zunahme jenes Elementes als seine Konzentration selbst.
Materialien und Apparatur
Der Versuchsorganismus, Chlorella vulgaris, wurde in Form einer Reinkultur erhalten * und gezüchtet in einer Nährlösung nach Kuhl10, mit einem auf 1/10 erniedrigten Gehalt an Magnesium11. Der weggefallene Teil des Magnesiums wurde ersetzt durch eine äquimolekulare Menge Natriumsulfat.16 Das Wachstum der Algen wurde gefördert durch Überleitung eines Gemisches von Luft mit 5% Kohlendioxid und Beleuchtung mit einer 150 W Lampe in einer Höhe von ca. 50 cm über den Kulturen. – Die Herstellung der Nährlösung, die Impfung, Verdünnung usw. geschahen unter sterilen Bedingungen.
Die sechst Versuchskulturen befanden sich in flachen Quarzschalen (“Vitreosil“, Durchmesser 10cm, Höhe 1.5 cm, Wandstärke 0.3 cm), die auf der durchlöcherten Grundplatte eines mit destilliertem Wasser bis zu dieser Platte aufgefüllten und auf 27° gehaltenen Schüttelbades (Dubnoff Incu-shaker, labline model 61) befestigt waren und wurden beim Schütteln mit einer Frequenz von 60 pro Minute und einer Amplitude von 3.5 cm hin und her bewegt. In jede Schale wurde 50 ml der Nährlösung einpipettiert und jeweils geimpft mit 2 ml einer vorher zubereiteten Chlorella kultur in derselben Lösung. Jede Schale war während der Versuche lose bedeckt mit einer Kappe aus durchsichtigem Kunststoff, die mit einer Bohrung für den Gaszufuhr versehen war. Die ganze Grundplatte mit allen Schalen war überdeckt von einer grösseren, mitbewegten Kappe aus Perspex. Dünne Schläuche aus weichem Kunststoff verbanden die Räume unter den einzelnen Schalenkappen mit einer Gasverteilungskammer, die in einer Bohrung der Perspexkappe befestigt war.
Das Gasgemisch wurde einem Vorratszylinder mit Reduzierventil entnommen, durch eine Gaswasflasche, welche die oben erwähnte Impfkultur enthielt und weiter durch ein Wattenfilter in die Verteilungskammer geleitet, aus dem es in langsamen Strom in die Räume über den Versuchskulturen eintrat. Durch die zwischengeschaltete Kultur in der Gaswasflasche wurde während jeder Wachstumsperiode die Impflösung für den nächsten Arbeitsgang bereitet. Ausserdem diente sie zur teilweisen Kompensation der Verdampfung aus den Schalen.
Verlauf des Versuchs
Das Wachstum der Algen konnte in den Teilversuchen durch Vergleichung mit der ursprünglichen Impfkultur ad oculos verfolgt werden. In den ersten drei Wachstumsperioden war es durchaus befriedigend, in den letzten drei wurde es geringer. Ausserdem änderte sich hier das Aussehen der Suspension: es bildeten sich Klumpen von Zellen, und die Farbe wurde dunkler. Das gleiche wurde beobachtet in den zugehörigen Impfkulturen. In den letzteren konnte durch Bestimmung des Chlorophyllgehaltes (siehe Analytische Methoden) der Gehalt an Algen auch quantitativ im Verhältnis zum Gehalt der ursprünglichen Kultur ermittelt werden. Es schwankte zwischen 106-120% in den 6 nach einander verlaufenen Wachstumsperioden von 10 bis 14 Tagen.
Die Wiederherstellung der ursprünglichen Bedingungen nach jeder Wachstumsperiode geschah für die Versuchs- sowie für die Kontrollschalen in erster Linie durch Ansäuern mit 10ml 0.IN Salpetersäure und Eindampfen unter einem Rotstrahler. Der Trockenrest verkohlte und verbrannte dabei bereits zum Teil; eine kurze Erhitzung im Glühofen war aber unumgänglich zur vollständigen Veraschung (10 Min. bei 500-520°). Dabei findet durch doppelte Umsetzung der anwesenden sauren Phosphate mit den Nitraten eine Alkalisierung statt, die durch eine Behandlung der Asche mit verdünnter Salpetersäure (10 ml 0.0IN) bei mässiger Hitze rückgängig gemacht werden konnte. Die Asche wurde schliesslich in 50 ml Wasser aufgenommen zu einer annähernd neutralen Nährlösung für die nächste Wachstumsperiode.12
In jedem Teilversuch wurde nach der letzten Wachstumsperiode die neutralisierte Asche in 5 ml 0.0IN Perchlorsäure aufgenommen, kurz auf dem Wasserbad erwärmt und nach Abkühlung auf 50 ml gebracht. Die Aschenlösungen wurden in gut verschlossenen Polyäthylenflaschen bei 4° aufbewahrt.
Analytische Methoden
Kalium wurde zuerst bestimmt nach Flaschka durch Titrimetrie des unlöslichen Kaliumsalzes der Tetraphenylborsäure (Kalignost 13 ). Die Bestimmung geschah für jede Aschenlösung fünffach. Jedes Paar Versuchs- und Kontrollaschenlösungen wurde im selben Arbeitsgang analysiert, ausserdem in den meisten Fällen gleichzeitig mit der ursprünglichen Nährlösung und einer Eichlösung, die Kaliumchlorid in genau bekannter Konzentration (0.01 M) enthielt. Letztere lieferte als Ergebnis der Bestimmung im Mittel 1.000x10-2.M (n=0.018 x 10-2), die Nährlösung im Mittel 0.985 x 10-2 M (n=15, s=0.018 x 10-2).
Kalium und Natrium wurden weiter bestimmt mittels Flamenfotometrie (Corning 400 Flame Photometer).** Die Aschenlösungen wurden zu diesem Zweck auf 1/100 verdünnt; die dabei resultierenden Konzentrationen (K± 4ppm, Na ± 2 pp) liegen unterhalb der Grenze der Querempfindlichkeit beider Elemente und im Bereich der linearen Abhängigkeit des Fotometerwertes von der Konzentration.
Der Chlorophyllgehalt der Impfkulturen wurde ermittelt durch Zentrifugieren eines bestimmten Volumens, wiederholte Extraktion des Zentrifugats mit Methanol bei 70° und Kolorimetrie der erhaltenen Chlorophyll-Lösungen bei 660 nm.14, 15
Ergebnis des Versuchs und Diskussion
Die für den Kalium- und Natriumgehalt der Aschenlösungen gefundenen Werte sind in den Figuren 1, 2, und 3 dargestellt. In Fig. 1 ist ausserdem die Streuung17 der gefundenen Analysenwerte um ihr Mittel angegeben. Das Verhältnis K : Na ist in Fig. 4 wiedergegeben; es wurde erhalten als der Quotient der für die beiden Elemente durch Flammenfotometrie ermittelten Konzentrationen. Das Bild ist nicht wesentlich anders, wenn man für den Kaliumgehalt den nach der Kalignostmethode erhaltenen Wert einsetzt.
In jeder Figur ist auf der X-Achse die Nummer der einzelnen Teilversuche und damit die Anzahl der in jedem Teilversuch durchlaufenen Wachstumsperioden eingetragen. Der Y-Wert bedeutet in Fig. 1 die Konzentration der Aschenlösungen; in den anderen Figuren sind die Analysenwerte dieser Lösungen, resp. Die Werte für das Verhältnis K : Na immer in Prozenten der für die Nährlösung gefundenen angegeben. Der Y-Wert für X = 0 bezieht sich in allen Figuren af die unveränderte Nährlösung.
Es ist zu beachten, dass bei jedem folgenden Teilversuch der Gehalt der Aschenlösungen in allen Bestandteilen um 4% zu steigen hätte, weil mit jeder Impfung dieselbe Menge Impfkultur (2 m.) zur Nährlösung (50 ml) hinzugefügt wurde und das Endvolumen der Aschenlösung immer dasselbe war (50 ml). Der dementsprechend zu erwartende Verlauf der Konzentrationen ist in Fig. 1, 2, 3 durch eine gestrichelte Gerade angegeben.
Als Hauptergebnis der Wachstumsversuche ist das auffallende Defizit an Kalium im Vergleich mit den Kontrollversuchen zu betrachten (Fig. 1 - 2), das sch in zunehmendem Masse in den ersten vier Teilversuchen zeigt, in de letzten zwei aber nicht festzustellen ist. Es beträgt bei den Analysen nach der Kalignostmethode (Fig. 1) maximal 14%, minimal –2%, im Mittel 4% und ist wenigstens für den vierten Teilversuch als signifikant mit Bezug auf die analytische Präzision zu betrachten. Für die Flammenfotometrisch erhaltenen Werte (Fig. 2) sind die zugehörigen Beträge : 25%, -4%, +8%.
Im Verglich zum Kalium weichen die Werte für den Natriumgehalt der Versuchskulturen in unsystematischer Weise von den Kontrollwerten ab, wobei die Differenz zwischen +6 und –6 schwankt und im Mittel ein Überschuss von 1% in den Versuchskulturen gefunden wurde. Der Befund dieser verhältnismässig geringen mittleren Abweichung kann als eine Stütze betrachtet werden für die Annahme, das Natrium dem Erhaltungsgesetzt folgt und daher als interner Standard verwendbar ist.
Die Konsequenz dieser Annahme ist, dass das Verhältnis K – Na konstant und gleich dem der Nährlösung sein muss, insofern keine spezifisch den Kaliumgehalt ändernde Einflüsse wirksam sind (s. S. 3).
In der Tat zeigen die Werte für das Verhältnis K . Na (Fig 4) in den Kontrollen eine Abweichung von maximal 3%, im Mittel 1% von dem Wert für die ursprüngliche Nährlösung. Dagegen weist dieses Verhältnis für die ganze Reihe der Versuchskulturen ein Defizit bis um 15% auf.
Angesichts der Ungewöhnlichkeit dieses Ergebnisses kann es nur als ein vorläufiges betrachtet werden. Es könnte aber die Aufmerksamkeit hinlenken auf die Möglichkeit, dass im Laufe des organischen Entwicklungsprozesses das Element Kalium zuerst in Anderes umgesetzt und nachher wiederum zurückgebildet wird.
Es wird erhofft, durch eine erweiterte Untersuchung, unter verschärfter Wahrung vor Fehlerquellen eine Entscheidung über die Realität des gefundenen Kaliumschwundes zu erreichen. Sollte dabei das obige Resultat bestätigt werden, so eröffnet sich die Perspektive auf eine Modifikation unserer bisherigen Ansichten über die Unveränderlichkeit der Elemente, insoweit diese mit dem Lebensprozess der Pflanze verbunden sind.
Utrecht, Pathologisches Institut
Der Universität
April 1981
L. W. J. Holleman
Figuren
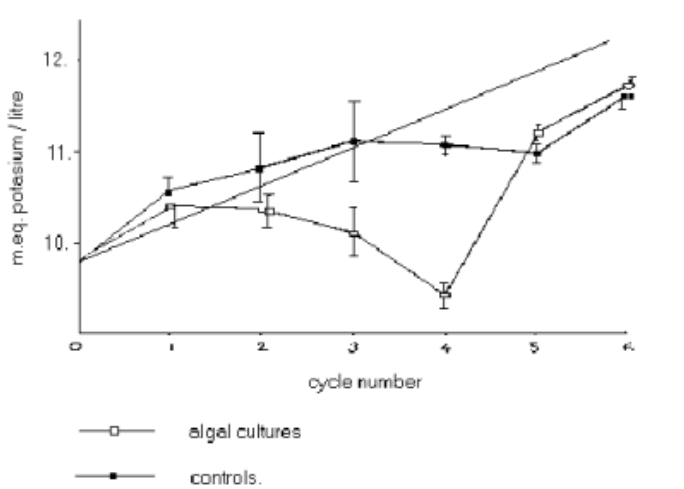
Figure 1: Potassium content of ash solutions by Kalignost method
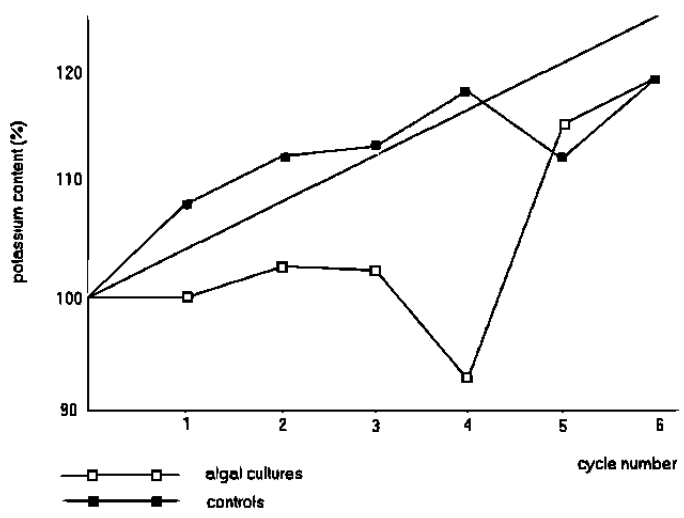
Figure 2: Potassium content of ash solutions by flame photometry
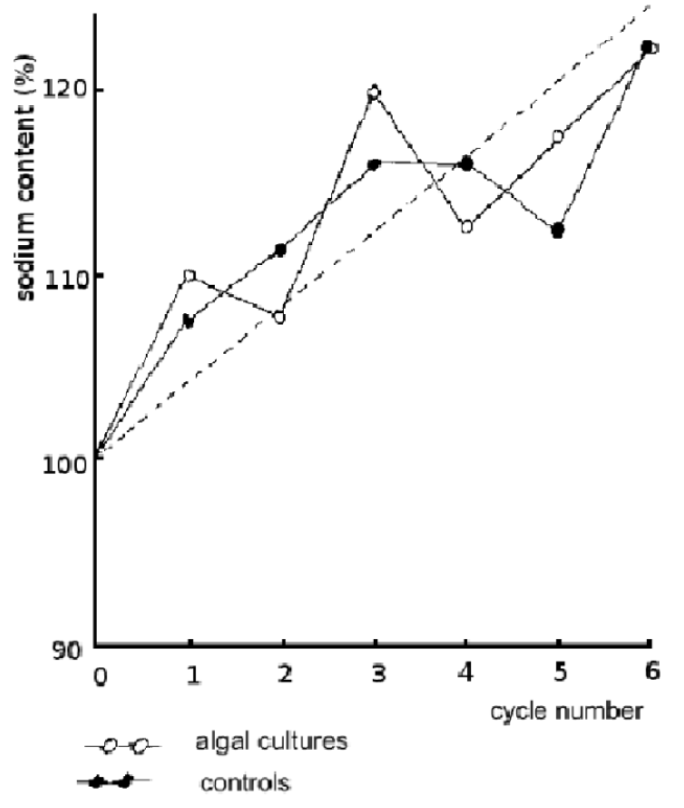
Figure 3: Sodium content of ash solutions by flame photometry
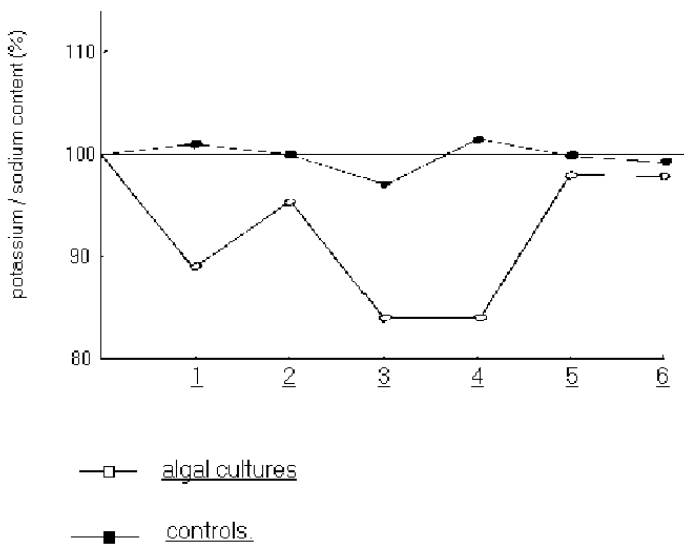
Figure 4: Ratio of potassium to sodium content of ash solutions by flame photometry
Literatur und Anmerkungen
- Wiegmann, A. F. und L. Polstorff, Über die anorganischen Bestandteile der Pflanzen, oder Beantwortung der Frage: Sind die anorganischen Elemente, welche sich in der Asche der Pflanze finden, so wesentliche Bestandteile des vegetabilischen Organismus, dass dieser sie zu seiner völligen Ausbildung bedarf, und werden sie den Gewächsen von aussen dargeboten? Braunschweig 1842, (in) Browne: A source Book of Agricultural Chemistry, Chron. Bot. 8, p. 220 (1944)
- Herzeele, A. von, Über die Entstehung der anorganischen Stoffe (u. drei weitere Abhandlung), Berling 1876-1883; (abgedruckt als Anhang in:) Hauschka, R.: Substanzlehre 7. Aufl., Frankfurt a. M. 1978 (Vittorio Klostermann).
- Kervran, L. C., La Transmutation biologique, Paris 1966 (Le Courier du Livre; engl. Uebersetzung: Biological transmutation, N.Y. 1972 (Swan House publishing Co.)
- Id. Geen leven zonder kosmische energie, Natura docet, Ned. Tijdschr. Natuurgeneesk. 27, 81 (1976)
- de Gee, J.C., Biologische Transmutaties, Chem. Weekbl. 69, 11 (1973)
- Goldfein, S., Energy development from elemental transformations in biological systems, U.S. Army mobility equipment Research and Development Command, Fort Belvoir, Viginia, Report 2247, 1978.
- Anderweitig zu veröffentlichen.
- Rudolf Steiner, Geisteswissenschaftliche Grundlagen zum Gedeihen der Landwirtschaft, Dornach, Schweiz, 1979, 5.Vortrag; Niederl. Ausgabe: Geesteswetenschappelijke grondslagen voor een vruchtbare ontwikkeling v. d. Landbouw, Zeist 1977 (Uitg. Vrij Geestesleven)
- Solche Volumänderungen sind wahrscheinlich aufgetreten im Laufe der Untersuchung: (a) in dem Teilversuch 5, wo durch eine Verzögerung des Schüttelrhythmus die Flüssigkeit in den betreffenden Schalen zeitweilig in unerwartet starker Wallung geriet; dieser Umstand erklärt wenigstens zum Teil die niedrigen Analysenwerte für die Teilversuche, wo eine leichte Erhöhung der Analysenwerte über den erwarteten gefunden wurde; trotz Lagerung der Aschenlösungen im Eisschrank in geschlossenen Polyäthylenflaschen, war eine geringe Verdampfung während der durch Umstände bedingten lange ausgezogenen Aufbewahrungszeit nicht ganz auszuschliessen.
- Kuhl, A., (in) Beiträge zur Physiologie u. Morphologie der Algen, Stuttgart 1962 (G. Fischer Verlag, p. 157
- Es wurde beim Entwerfen des Versuchs ausgegangen von der Hypothese, dass eine Transmutation an dem Magnesium, als Zentrum des für die Assimilation benötigten Chlorophylls angreifen würden. Eine etwaige Änderung des Magnesiumgehaltes wäre dann bei reduziertem Gehalt der Nährlösung an diesem Element eher festzustellen sein.
- Der pH-Wert der in dieser Weise wiederhergestellten Lösungen wurde in besonderen Parallelversuchen kontrolliert.
- Flaschka, H., A. M. Amin u. A. Holasek, Eine neue methode zur massanalytischen Bestimmung von Kalium nach Fällung als Kalium tetraphenylborat, Z. anal. Chem. 138, 241, (1953)
- Boney, A.d., Phytoplankton (Studies in Biology no. 52), Glasgow 1974 (Edw. Arnold).
- Hille, J.C. van, The quantitative relation between rate of photosynthesis and chlorophyll centent in Chlorella pyrenoidosa. Recl. Trav. Botan. Neerl. 35, 688 (1938).
- Ibid., P. 708
- de Gee, J.C., Biologische Transmutaties, Chem. Weekbl. 69, 11 (1973)